江苏苏州工业园区九章路68号 中锐具美大厦9F
医学资讯
mRNA疫苗成全球首款正式获批新冠疫苗,国内上市进展如何?

当地时间8月23日,全球有了首个正式获批、拥有完整三期临床数据的新冠疫苗。
当天,美国食品和药物管理局(FDA)批准辉瑞及BioNTech共同研发的mRNA新冠疫苗(商品名COMIRNATY)的生物制品许可证申请(BLA)。
这是首款获FDA正式批准的新冠疫苗。获批后,它将用于16岁及以上人群预防新冠病毒感染。我国复星医药参与了此款疫苗的联合研发过程,其在中国香港及澳门地区的商品名为复必泰。
同时,该疫苗仍具有紧急使用范围(EUA),适用于12岁-15岁人群接种,以及某些免疫功能低下者加强接种(第三剂)。EUA是一种美国法律机制,是FDA在突发公共卫生事件下特殊的药品审核通道。
路透社援引白宫首席医疗顾问安东尼·福奇发言称,mRNA新冠疫苗(COMIRNATY)正式获批,将为更多人接种铺平道路。“如果绝大多数美国民众都接种了疫苗,美国就能控制住新冠疫情,并在2022年春前恢复正常。”
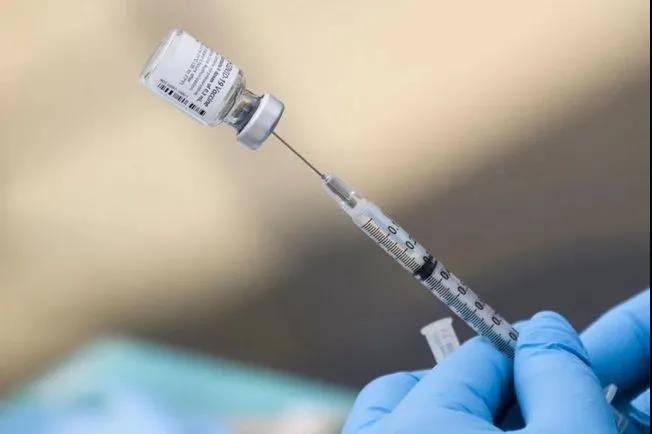
图片来源于AFP
为正式获批 ,报告达34万页
2020年12月11日,美国FDA批准前述疫苗的EUA申请。
为正式获批,今年5月7日,该疫苗研发机构向FDA递交一份综合数据包,达34万页。包括4.4万人长期研究数据,接种第二针后6个月的疗效和安全性数据,及许可所需的生产和设备数据。FDA资料显示,该款疫苗预防新冠感染有效率达到91%,预防重症感染率达95%。
《华尔街日报》称,FDA原计划在9月6日批准全面授权。但由于疫情形势严峻,卫生官员受到来自科学界和疫苗倡导团体的诸多压力,于是加速审批。
根据Worldometer实时统计数据,截至北京时间8月25日6时30分左右,美国累计确诊新冠肺炎病例38,912,537例,累计死亡647,913例。最近几周,受新冠病毒变异株德尔塔重创的一些地区,疫苗接种率得到提升。BBC称,这是民众对新冠疫苗信心增强的一种体现。
根据《新英格兰医学杂志》7月中旬发布的一项研究,前述mRNA新冠疫苗对德尔塔变异株有症状感染的预防效果达88%。
“在接种新冠肺炎疫苗方面,没有时间可以浪费。请大家今天就完成疫苗接种。”美国总统拜登表示。

图片说明:当地时间8月23日,美国纽约一个新冠疫苗接种点外,人们排队等候接种。/新华社
部分地区或行业将“强制接种”
根据美国疾病控制和预防中心数据,美国已接种2.04余亿剂次新冠疫苗。
CNBC报道,正式获批对疫苗接种将产生诸多实际影响。比如,研发企业将能在媒体上打广告,直接向消费者宣传、销售疫苗,并根据市场需求定价。即使疫情结束,相关疫苗仍可在市场销售。
更重要的是,这将推动“强制接种”。
路透社报道,根据EUA,民众必须被告知疫苗的获益和风险,主动选择接受或拒绝。但获FDA正式批准后,各州政府可以将接种疫苗,作为就业或教育的附加条件。
五角大楼发言人约翰·柯比说,国防部长劳埃德·奥斯汀正在兑现其本月早些时候所说,即一旦FDA完全批准,就强制要求130万现役军人接种。“五角大楼正在制定相关指南,将在未来几天提供时间表。”
部分地方政府和企业也已发出“强制接种”声明。纽约市市长比尔·德布拉西奥23日宣布,该市所有公立学校教师和其他公职人员必须在9月27日前,接种至少一剂新冠疫苗。芝加哥市市长洛丽·莱特富特当天宣布,要求市政员工接种疫苗,但未说明接种期限。
许多大型公司,如迪士尼、沃尔玛等,已官宣称全部或部分员工需在今秋完成接种。摩根士丹利和花旗银行表示,接种过疫苗的人才能回办公室。而纽约证券交易所已强制交易大厅人员接种。
这还有助于消除一部分“接种犹豫”。美国凯撒家庭基金会6月底发布民意调查数据显示,约30%未接种者表示,若疫苗获得FDA正式批准,他们将更有可能接种疫苗。在对疫苗采取观望态度的人群中,这一数字升至50%。
中国或实现“本土化”
FDA生物制品评估与研究中心主任彼得·马克斯称:“我们的科学和医学专家对这款疫苗进行了极其彻底和深思熟虑的评估。我们评估了数十万页的科学数据和信息,对COMIRNATY的安全性和有效性进行分析,并对生产过程进行了详细评估,包括对生产设施的检查。新冠疫情持续,公众期待安全有效的疫苗。公众和医学界可以相信,尽管我们很快批准了这种疫苗,但它完全符合美国现有的疫苗高标准。”
“今天FDA的正式批准,强调了该疫苗良好的疗效和安全性。我们已经向全世界输送了超过10亿剂疫苗。我们将继续不懈地努力,扩大疫苗的使用范围,并为可能出现的逃逸变种做好准备。”BioNTech首席执行官兼联合创始人Ugur Sahin博士表示。
BioNTech是前述疫苗美国、欧盟和英国的上市许可持有人。在大中华地区,复星医药早在2020年3月16日就和BioNTech宣布达成战略合作协议,复星医药获BioNTech授权,在中国大陆及港澳台地区独家开发、商业化基于其专有mRNA技术平台研发的、针对新冠病毒的疫苗产品。
在全球联合研发过程中,复星医药在临床研究、药理数据、药物警戒等多方面,与BioNTech进行深度合作。该款mRNA新冠疫苗研发成功,包含中国科研团队的智慧。
2021年上半年,该款疫苗已获得中国香港紧急使用认可和中国澳门的特别许可进口批准,并已投入中国香港和澳门地区的接种计划。根据复星医药8月23日披露的2021年半年报显示,截止8月20日,该疫苗在中国香港及中国澳门分别累计接种431.4万剂和8.7万剂。
据了解,该疫苗在中国境内(不包括港澳台)处于II期临床桥接试验阶段,并已滚动提交了包括全球III期临床数据在内的相关数据,这款疫苗国内附条件上市的审批工作在正常推进中。此前在2021年5月9日,复星医药发布公告称,其控股子公司复星医药产业拟与BioNTech投资设立合资公司,以实现mRNA新冠疫苗产品的本地化生产及商业化。据公告,复星医药将提供年产能可达10亿剂mRNA新冠疫苗的生产设施。
一旦审批通过,复星医药和BioNTech将迅速推动国内本土化生产,成为国产化的mRNA新冠疫苗。
来源:医声医事
资料来源:
1.Pfizer-BioNTech COVID-19 Vaccine COMIRNATY® Receives Full U.S. FDA Approval for Individuals 16 Years and Older. BioNTech
2.FDA grants full approval to Pfizer/BioNTech Covid-19 vaccine, opening door to more vaccine mandates. CNN
3.FDA Approves First COVID-19 Vaccine. FDA
4.US Covid-19 vaccine approval is 'seismic' shift for legality of mandates, experts say. Reuters
5.US could control Covid by spring 2022 if more people get shots: Fauci. Reuters
6. Pfizer-BioNTech COVID-19 Vaccine Frequently Asked Questions. FDA
7.辉瑞/BioNTech成为首款获美国全面授权疫苗 是否意味强制接种?BBC

